在国家重大科学研究计划支持下,中国科学院武汉病毒研究所龚鹏研究员团队,利用时间分辨晶体学方法较完整地揭示了RNA病毒聚合酶核苷酸添加循环的结构基础,发现了这类聚合酶催化中心关闭的独特模式和在RNA上转位的独特机制。在该类聚合酶关闭催化中心的过程中,一对独特的天冬氨酸-丝氨酸组合与NTP底物核糖环上的2?位羟基发生协同构象变化并建立一个新的氢键网络,这一发现对研制靶向RNA病毒聚合酶的核苷类药物提供了重要线索(图一)。在该类聚合酶的转位过程中,模板-产物RNA双链被观测到以不对称方式向上游转位,且控制转位的聚合酶元件与控制催化的聚合酶元件相对独立,明确不同于其他类别的核酸聚合酶,这一发现为通过精准控制聚合酶转位过程来实现病毒复制效率调控提供了理论基础,为理性化设计减毒疫苗提供了新策略。
相关研究工作发表在美国科学院院刊PNAS上(Shu and Gong, PNAS 2016),并获RNA Biology和Viruses杂志邀请分别撰写了综述论文。
附图:

图一:RNA病毒聚合酶独特的催化机制(A)利用时间分辨晶体学方法捕获聚合酶核苷酸添加循环中的多个状态。(B)电子密度显示底物NTP的碱基部分首先与模板核苷酸发生相互作用。(C)该类聚合酶所独有的天冬氨酸-丝氨酸对(D238-S289)在催化中心关闭过程中发挥核心作用。
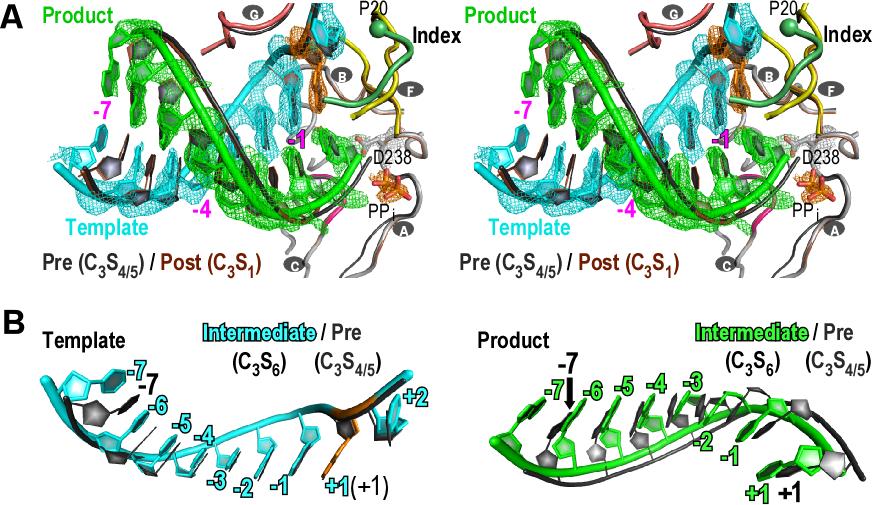
图二:RNA病毒聚合酶独特的转位机制(A)转位过程中模板-产物RNA链发生不对称运动。(B)产物RNA链向上游移动的幅度显著领先于模板RNA链。
